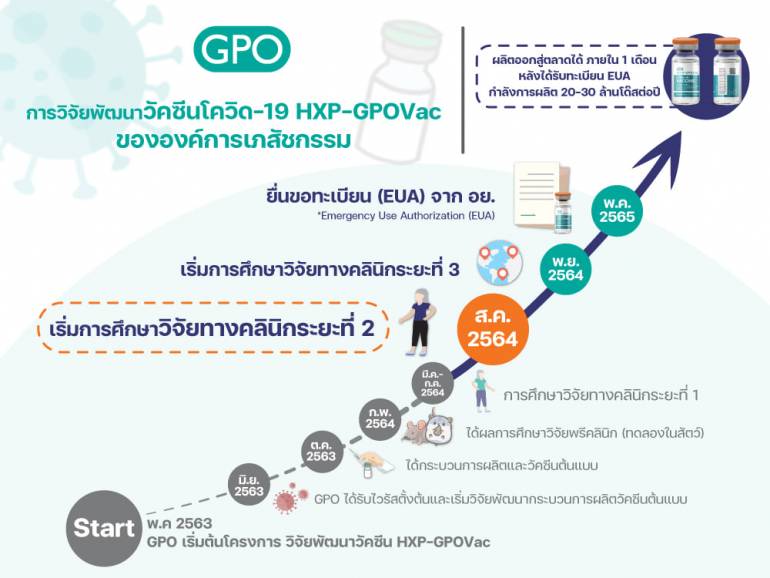
วันที่ 16 ส.ค.2564 นพ.วิฑูรย์ ด่านวิบูลย์ ผู้อำนวยการองค์การเภสัชกรรม (อภ.) กล่าวว่า หลังจาก อภ.ได้ดำเนินการวิจัยพัฒนากระบวนการผลิตวัคซีน และได้ทำการผลิตวัคซีนป้องกัน COVID-19 "HXP–GPOVac" จนสำเร็จในขั้นแรก และนำเข้าสู่ขั้นตอนของการศึกษาวิจัยในมนุษย์ นับเป็นวัคซีนโควิดชนิดแรกของประเทศไทยที่ได้วิจัยในมนุษย์
ขณะนี้การศึกษาวิจัยในมนุษย์ในระยะที่ 1 ได้ผลการวิเคราะห์ภูมิคุ้มกันที่ 14 วัน หลังจากได้รับวัคซีนครบ 2 เข็มแล้ว เมื่อวันที่ 16 ส.ค. ได้เริ่มทำการศึกษาวิจัยในมนุษย์ระยะที่ 2 โดยวิจัยในอาสาสมัคร จำนวน 250 คน อายุ 18-75 ปี ที่มีสุขภาพดี ไม่เคยฉีดวัคซีนป้องกัน COVID-19 ทุกชนิดมาก่อน และไม่เคยเป็นผู้ป่วยมาก่อน โดยการศึกษาวิจัยในมนุษย์ระยะที่ 1 และ 2 นี้ อภ.ได้ให้คณะเวชศาสตร์เขตร้อน มหาวิทยาลัยมหิดล เป็นผู้ดำเนินการศึกษาวิจัย โดยมี ศ.พญ.พรรณี ปิติสุทธิธรรม หัวหน้าภาควิชาอายุรศาสตร์เขตร้อน รักษาการหัวหน้าศูนย์วัคซีน คณะเวชศาสตร์เขตร้อน มหาวิทยาลัยมหิดล เป็นหัวหน้าโครงการศึกษาวิจัยในมนุษย์ครั้งนี้

นพ.วิฑูรย์ กล่าวว่า อภ.ได้พัฒนาวัคซีน HXP–GPOVac โดยการสนับสนุนจากองค์กร PATH ที่ได้ส่งมอบหัวเชื้อวัคซีนต้นแบบซึ่งพัฒนาโดยโรงเรียนแพทย์ที่เมาท์ไซนาย (The Icahn School of Medicine at Mount Sinai) และมหาวิทยาลัยเท็กซัสที่ออสติน (University of Texas at Austin) ประเทศสหรัฐอเมริกา มาทำการผลิตที่โรงงานผลิต (วัคซีน) ชีววัตถุ ของ อภ. ที่ ต.ทับกวาง อ.แก่งคอย จ.สระบุรี ซึ่งได้มีการวิจัยพัฒนากระบวนการผลิตและสามารถผลิตวัคซีน HXP–GPOVac จากนวัตกรรมเชื้อตายชนิดลูกผสม (Inactivated chimeric vaccine) ผลิตด้วยเทคโนโลยีไข่ไก่ฟัก (Egg-based) เช่นเดียวกับการผลิตวัคซีนไข้หวัดใหญ่ และนำเข้าสู่กระบวนการวิจัยในมนุษย์ได้สำเร็จในระยะเวลา 10 เดือน
เมื่อการศึกษาวิจัยในมนุษย์ครบทั้ง 3 ระยะและได้รับการขึ้นทะเบียนตำรับ เพื่อใช้ในกรณีฉุกเฉิน (Emergency Use Authorization, EUA) จากสำนักงานคณะกรรมการอาหารและยา (อย.) สำเร็จ คาดว่าจะเริ่มผลิตได้ในกลางปี 2565 โดยจะสามารถผลิตได้ 20-30 ล้านโดสต่อปี และจะทำการขยายกำลังการผลิตอย่างต่อเนื่อง ในเบื้องต้นนี้ “วัคซีน HXP–GPOVac” จะสามารถรองรับการฉีดเพื่อป้องกัน COVID-19 ให้ชาวไทยได้ 10-15 ล้านคน

ขณะที่ ดร.ภญ.พรทิพย์ วิรัชวงศ์ หัวหน้าโครงการ “วัคซีน HXP–GPOVac” องค์การเภสัชกรรม กล่าวว่า หัวเชื้อวัคซีนต้นแบบนี้ ได้พัฒนาจากนวัตกรรมการตัดต่อไวรัสนิวคาสเซิล (Newcastle disease virus, NDV) ให้มีการแสดงออกของโปรตีนหนามของไวรัสโคโรนาที่ได้ถูกปรับแต่งด้วยเทคโนโลยีเฮกซะโปร (HexaPro) ให้มีความคงตัวมากขึ้น มาใช้ในการกระตุ้นร่างกายให้สร้างภูมิคุ้มกันต้าน COVID-19 เทคโนโลยีเฮกซะโปรนี้ ถูกพัฒนาที่มหาวิทยาลัยเท็กซัสที่ออสติน โดยนักวิจัยกลุ่มเดียวกับที่ได้พัฒนาโปรตีนหนามรุ่นแรกที่ใช้ในวัคซีน COVID-19 อย่างน้อย 3 ชนิดที่มีการใช้อยู่ทั่วโลก โดยทั้งนี้องค์กร PATH ได้ส่งมอบหัวเชื้อไวรัส ให้แก่ 3 ผู้ผลิตวัคซีนในประเทศเวียดนาม ประเทศบราซิล รวมทั้งองค์การเภสัชกรรมของประเทศไทยด้วย “วัคซีน HXP–GPOVac” นับเป็นความมั่นคง ลดการนำเข้า และเป็นการพึ่งพาตนเองด้านวัคซีนของประเทศอย่างยั่งยืน และยังส่งผลต่อความมั่นใจในการดำเนินชีวิตและการขับเคลื่อนเศรษฐกิจของสังคมไทย
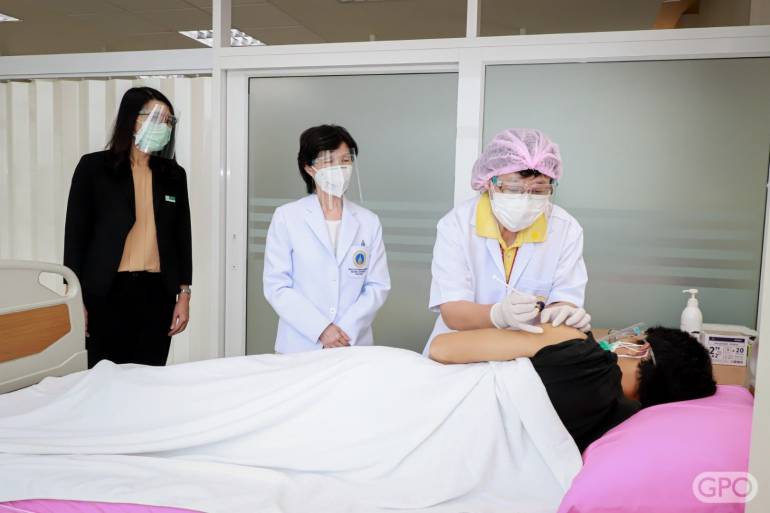
ทั้งนี้ ผู้ที่ได้รับวัคซีนจะมีอาการไม่พึ่งประสงค์ไม่รุนแรง เช่น ปวดกล้าม ปวดหัว เพียงระยะหนึ่งแล้วหาย ส่วนผลการกระตุ้นภูมิคุ้มกัน พบว่าวัคซีนสามารถกระตุ้นภูมิคุ้มกันและยับยั้งไวรัสได้ในระดับที่น่าพอใจ และผ่านเกณฑ์เข้าสู่การศึกษาวิจัยในระยะที่ 2 นอกจากนี้ จะศึกษาวิจัยเกี่ยวกับการกระตุ้นบูสเตอร์โดส และการยับยั้งเชื้อกลายพันธุ์ เนื่องจากในอนาคตอาจมีสายพันธุ์ใหม่เกิดขึ้น